
Is het periodiek systeem compleet?
Wat zijn elementen?
Voordat het periodiek systeem wordt bedacht, wordt eerst een andere belangrijke scheikundige ontdekking gedaan: het bestaan van de elementen.
De oude Grieken geloven al in het bestaan van elementaire deeltjes waaruit alles is opgebouwd. Zij hebben het over de elementen vuur, aarde, lucht en water. Ook spreken zij over als vijfde element. De Franse scheikundige Antoine Laurent Lavoisier (1743 - 1794) haalt dit idee onderuit door te bewijzen dat water te ontleden is in nóg kleinere deeltjes en daarom dus geen element is. Dat laat hij zien met een experiment, waarmee hij aantoont dat water bestaat uit de elementen waterstof (H) en zuurstof (O).
Waar komt het periodiek systeem vandaan?
Het is onmogelijk om waterstof en zuurstof in nog kleinere stukjes te ontleden zonder dat ze hun kenmerkende eigenschappen (dus dat wat ze waterstof en zuurstof maakt) verliezen. Dat zie je ook terug in de definitie van Lavoisier. Hij beschrijft elementen als stoffen die niet verder chemisch te ontleden zijn. Elementen kunnen wel als bouwstenen dienen voor andere stoffen, ook wel moleculen genoemd, zoals watermoleculen en alcoholmoleculen. In essentie blijven de losse bouwstenen binnen zo’n stof altijd behouden. En ze kunnen dan ook altijd als aparte elementen worden teruggewonnen uit deze moleculen. Uit water kunnen dus altijd de elementen waterstof en zuurstof worden gewonnen.
Een element is een soort atoom. Atomen bestaan uit een kern, met daaromheen elektronenschillen. In een kern zitten (positief geladen) protonen en (neutrale) neutronen. Om de kern heen ‘vliegen’ (negatief geladen) elektronen. Het is te vergelijken met het zonnestelsel: om de zon draaien allemaal planeten in hun eigen baan. Bij een atoom zie je dat ook. Om de kern, die is opgebouwd uit protonen en neutronen, draaien allemaal elektronen in verschillende banen, elektronenschillen genoemd.
Het aantal protonen en elektronen in atomen van dezelfde soort is precies gelijk. De samenstelling van deze deeltjes binnen een atoom bepaalt welk element het atoom is. Zo is een atoom met één proton en dus één elektron het element waterstof, maar is een atoom met 79 protonen en dus 79 elektronen het element goud.
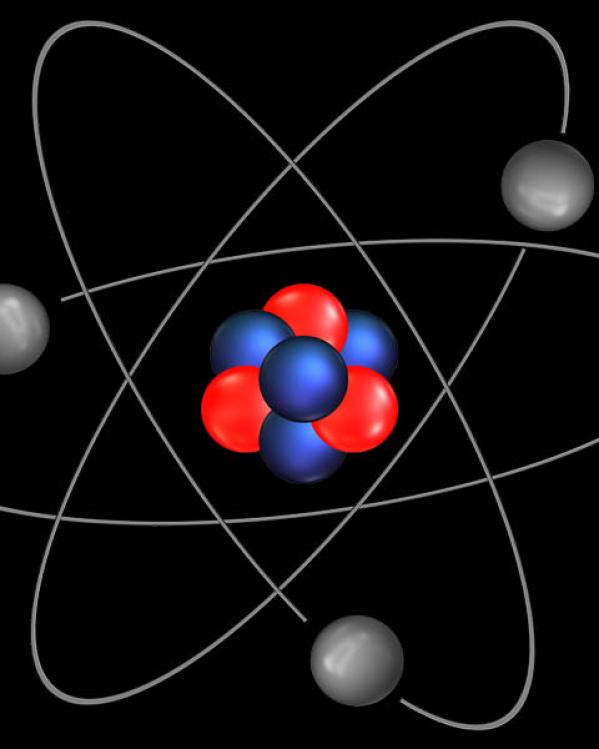
Schematische weergave van een lithiumatoom.
Wat is het periodiek systeem?
Het periodiek systeem der elementen is een schematisch overzicht van alle 118 bekende elementen. Het schept een logisch, geordend overzicht van deze elementen op basis van hun specifieke eigenschappen. De bekende Engelse wetenschapper en schrijver C.P. Snow omschreef het nut van het periodiek systeem als volgt: “Voor het eerst zag ik een samenraapsel van willekeurige feiten samenvallen in een logische volgorde. Alle wetenswaardigheden en formules van de scheikunde zoals ik die ken uit mijn jeugd, leken zich voor mijn ogen ineens in het schema in te passen – alsof je voor een jungle staat die plotseling verandert in een keurige tuin.”
Het periodiek systeem wordt vaak vergeleken met ons alfabet. De 26 letters uit dit alfabet kun je combineren tot een oneindig aantal mogelijke woorden. Woorden variëren in lengte, het aantal keer dat dezelfde letter erin voorkomt, enzovoorts. Dat geldt eigenlijk ook voor het periodiek systeem, waar de letters in deze vergelijking staan voor de afzonderlijke elementen.

De elementen worden in het systeem weergegeven met een hoofdletter, die in de meeste gevallen wordt gevolgd door een kleine letter. De afkorting He staat bijvoorbeeld voor helium, Na voor natrium en Al voor aluminium. Met die elementen kun je alle mogelijke soorten materie maken die er bestaan. Bekende combinaties van elementen zijn bijvoorbeeld H2O (water), dat bestaat uit de elementen waterstof (H) en zuurstof (O), en NaCl (keukenzout), dat bestaat uit de elementen natrium (Na) en chloor (Cl). Langere combinaties zijn ook mogelijk. Bekende voorbeelden zijn H2SO4 (zwavelzuur) en C2H5OH (alcohol). De cijfertjes die je in sommige namen ziet staan, staan voor het aantal atomen dat voorkomt in de combinatie. Zo komen in water twee atomen waterstof en één atoom zuurstof voor. Van alle elementen komen alleen de eerste 94 uit het periodiek systeem voor op aarde. De rest, nummers 95 tot 118, kunnen alleen gesynthetiseerd worden in een laboratorium.
Titine
Een bijzonder molecuul is titine. Het is het grootst bekende eiwit, met als chemische formule C169718H270459N45687O52243S913. De chemische naam van het eiwit is ook het langste woord ter wereld: het bestaat uit 189.819 letters en kost 3,5 uur om voor te lezen.
Wie voor het eerst een periodiek systeem voor ogen krijgt, kan waarschijnlijk niet meteen een logica ontdekken in de volgorde van de elementen. Die logica is er wel degelijk: zowel gezien vanuit de rijen als vanuit de kolommen volgt het ene element op een logische manier op het andere.
Een handige uitleg van de elementen en hun toepassing vind je hier.
Diederik Jekel noemt het hele periodiek systeem uit zijn hoofd op.
Wat is er zo logisch aan het periodiek systeem?
De logische ordening maakt het periodiek systeem een belangrijk handvat voor scheikundigen. Als het periodiek systeem niet bestond, zou je van elk element apart de eigenschappen moeten opzoeken. Nu vertelt één blik op dit systeem je heel veel over een element. Je kunt er op drie verschillende manieren naar kijken: naar de kolommen, naar de rijen en naar de verschillende kleuren.
Zo hebben elementen in één kolom, ook wel groep genoemd, allemaal hetzelfde aantal elektronen in hun buitenste schil. Dat aantal loopt op van links naar rechts. Als je weet hoe hoog dit aantal voor elke groep is, weet je dus hoeveel elektronen elk element in die groep in zijn buitenste schil heeft. Dit aantal zegt je weer iets over hoe goed de elementen reageren met andere elementen (dus: hoe goed ze moleculen vormen met andere elementen).
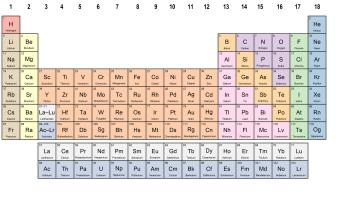
In de rijen, ook wel perioden genoemd, zijn de elementen gerangschikt op atoomnummer. Dat atoomnummer geeft het aantal protonen in de kern weer, dat gelijk is aan het aantal elektronen verdeeld in de schillen om de kern heen. Het aantal protonen, neutronen en elektronen in het atoom bepalen de zogeheten atoommassa van een element. Ook is aan de perioden af te lezen hoeveel schillen rond de kern zijn opgevuld met elektronen. Dat kunnen er maximaal zeven zijn, wat verklaart waarom de perioden oplopen van één tot en met zeven.
Op een afbeelding van het periodiek systeem zijn daarnaast verschillende gebieden te zien, die elk een andere kleur hebben. Elke kleur vertegenwoordigt een reeks elementen die als een groep bij elkaar horen. Zo zijn er de metalen, edelgassen en niet-metalen. Het grootste deel van de elementen bestaat uit metalen.
Wie bedacht het periodiek systeem?
Verschillende scheikundigen hebben zich beziggehouden met het maken van een bepaalde ordening van de elementen. De eer voor het bedenken van het periodiek systeem gaat echter naar de Rus Dmitri Mendelejev (1834-1907). Wanneer hij in 1863 in Sint-Petersburg als hoogleraar in de chemie les gaat geven, ontbreekt volgens hem een studieboek dat de principes van de algemene scheikunde goed uitlegt. Daarom besluit hij het zelf te schrijven. Tijdens het schrijven van dit werk, Principles of Chemistry, bedenkt hij in 1869 een ordening van de elementen die op dat moment bekend zijn. Hij schrijft de elementen en hun eigenschappen op aparte kaartjes en probeert ze zo te rangschikken. Hij ontdekt dat er een logische volgorde te maken is en is meteen overtuigd van zijn eigen gelijk:
Ik heb nooit getwijfeld aan de algemeenheid van deze wet, omdat het onmogelijk toeval kon zijn.

Dmitri Ivanovitsj Mendelejev (1834-1907)
Mendelejev is de eerste die de logische volgorde van groepen en perioden, zoals hierboven omschreven, toepast. De elementen zet hij op basis van hun atoommassa van laag naar hoog achter elkaar. Het knappe van het bedenken van deze rangschikking is dat hij met een beperkt aantal elementen (er zijn dan maar een paar elementen bekend) het bestaan van nog te ontdekken elementen kan voorspellen. In zijn logische volgorde zitten namelijk nog wat gaten. Pas jaren later, in 1875, wordt het volgende element ontdekt dat precies past in één van deze gaten. Dat is het element gallium, ontdekt door de Fransman Paul Emile Lecoq. Als in 1879 en 1886 scandium en germanium worden ontdekt (door de Zweed Lars Nilson en de Duitser Clemens Winkler), wordt pas echt duidelijk dat het systeem van Mendelejev klopt. Desondanks duurt het nog vijftig jaar tot de volgende twee gaten die Mendelejev heeft aangeduid, worden opgevuld.
Ondanks zijn belangrijke bijdrage aan de scheikunde krijgt Dmitri Mendelejev nooit de Nobelprijs voor zijn ontdekking. Wel komt hem een andere, misschien wel nog grotere eer toe: atoom 101 is naar hem vernoemd met de naam mendelevium.
Wat is het verschil tussen oude en moderne periodiek systeem?
Het periodiek systeem zoals Mendelejev het bedacht ziet er iets anders uit dan het periodiek systeem dat vandaag de dag wordt gebruikt. Hoewel een aantal dingen hetzelfde is gebleven (rangschikken op eigenschappen, families en groepen), is er ook een en ander veranderd.
De belangrijkste verandering is die van de ordening van alle elementen. Mendelejev rangschikte de elementen op atoommassa. Deze volgorde wordt lang aangehouden, maar naarmate meer elementen worden ontdekt, blijkt met deze rangschikking de volgorde verticaal niet helemaal meer te kloppen. Normaal zouden namelijk alle atomen met dezelfde eigenschappen boven elkaar moeten staan, maar dat is ineens niet meer het geval. Besloten wordt de elementen niet te rangschikken op atoommassa, maar op atoomnummer. Dat staat voor het aantal protonen in de kern en is gelijk aan het aantal elektronen in de schil van het atoom. Met deze rangschikking klopt het periodiek systeem weer precies.

Het oude systeem van Mendelejev uit 1869.
Het aantal bekende elementen is sinds 1869 flink gegroeid; inmiddels staat de teller op 118 elementen. Wie oude foto’s ziet van de eerste versie van het periodiek systeem, zal opmerken dat het er nu iets anders uitziet. Mendelejev presenteert het verticaal, terwijl wij het nu horizontaal gebruiken.
Waarom kwam er een nieuw systeem?
Is het periodiek systeem compleet?
Op 30 december 2015 worden de laatste elementen aan het periodiek systeem toegevoegd. Het gaat om nummer 113, 115, 117 en 118. Is het periodiek systeem dan nu vol? Niet per se. In theorie is het mogelijk om het volgende element in de reeks, nummer 119, te maken in een laboratorium. Het maken van een nieuw element gebeurt door twee elementen met een hoge snelheid op elkaar af te vuren. Het aantal protonen in de kern bepaalt het atoomnummer, dus als je atoomnummer 119 wilt maken zal je twee elementen op elkaar af moeten vuren die bij elkaar precies 119 protonen hebben. Het nadeel: dat kost heel veel energie. Ook is zo’n element heel instabiel, waardoor het na het ontstaan bijna meteen weer uit elkaar valt. Toch proberen wetenschappers dit voor elkaar te krijgen in de hoop zo meer inzicht te krijgen in hoe verschillende elementen toegepast kunnen worden. Enkele bekende toepassingen van elementen die eerder zijn gevonden, zijn het gebruik van americium in rookmelders, en van californium in de medische wereld, bij bestraling van bijvoorbeeld baarmoederhalskanker of hersentumoren.
"Het is net alsof er een paar letters aan het alfabet zijn toegevoegd." De hele aflevering zien? Kijk op de website van De Kennis van Nu.
Ieder nieuw ontdekt element moet natuurlijk een naam krijgen. In het verleden zijn dezelfde elementen weleens op verschillende plekken rond dezelfde tijd ontdekt. Dan kon het gebeuren dat één element meerdere namen kreeg. Om dat te voorkomen, is er een periode ingesteld waarin namen kunnen worden voorgesteld. De ontdekker neemt daarin het eerste initiatief. Tot die tijd krijgt het element een tijdelijke naam. Zo heet element 113, voor het de definitieve naam nihonion krijgt, tijdelijk ununtrium: een verzonnen naam geïnspireerd op de Latijnse benaming voor de getallenreeks 1-1-3. In het Nederlands zou dit eeneendrie-um zijn.
Periodiek systeem - Elementen toepassingen
Het wordt gezien als een enorme eer als een scheikundig element wordt vernoemd naar jou of naar de instelling waarvoor je werkt. Grote wetenschappers uit het verleden zoals Einstein zijn op die manier ook vereeuwigd: zo bestaan er elementen met de naam einsteinium, nobelium, lawrencium en curium. Ook het nieuwe element 118, oganesson is vernoemd naar een wetenschapper: deeltjeswetenschapper Joeri Oganessian. Daarnaast worden elementen weleens vernoemd naar de stad of het land waarin ze zijn ontdekt, denk aan darmstadtium, germanium, scandium en californium. Dat geldt ook voor de elementen 113, 115 en 117 die nihonion (naar Nippon, Japans voor land van de rijzende zon), moscovium en tennessine zijn genoemd.
Het periodiek systeem is een schematische weergave van alle elementen die bestaan. De meeste elementen komen in de natuur voor, maar sommige zijn alleen in een laboratorium te maken.
Een element is het kleinst mogelijke deeltje van een stof dat niet verder ontleed kan worden zonder de specifieke eigenschappen van dat element te verliezen. Elementen vormen de bouwstenen voor alles wat er op aarde te maken is.
Het periodiek systeem is bedacht door de Rus Dmitri Mendelejev. Hij rangschikt de elementen op atoommassa. Met zijn slimme ordening van elementen kan hij op basis van eigenschappen van bestaande elementen zelfs voorspellen welke elementen nog ontdekt moeten worden.
Mendelejev ordent het periodiek systeem op atoommassa, maar als er meer elementen worden ontdekt blijkt deze volgorde niet meer te kloppen. Daarom staan de elementen in het moderne periodiek systeem geordend op atoomnummer, dat gelijk is aan het aantal protonen in de kern.
In 2015 worden de laatste gaten van het periodiek opgevuld met de ontdekking van atoom 113, 115, 117 en 118. Dit zijn synthetische elementen, wat wil zeggen dat ze geen van allen in de natuur voorkomen.






